- 特瑞普利单抗是欧洲首个且唯一获批用于鼻咽癌治疗的药物,填补了欧洲鼻咽癌的治疗空白
- 特瑞普利单抗是欧洲唯一用于不限PD-L1表达的晚期或转移性食管鳞癌一线免疫治疗药物
- 继中国和美国之后,特瑞普利单抗的全球商业化布局正式向欧洲拓展
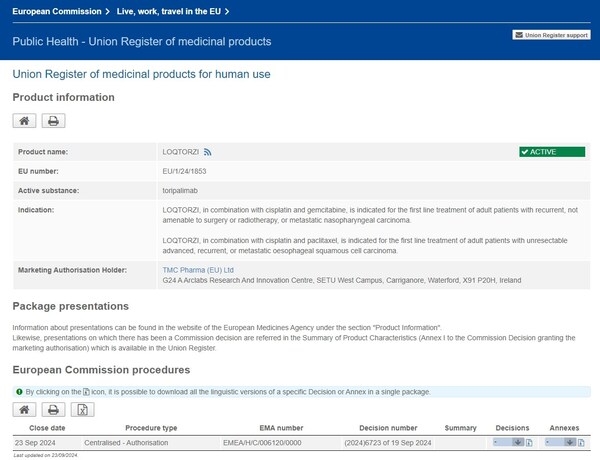
上海2024年9月24日 /美通社/ -- 北京时间2024年9月24日,君实生物(1877.HK,688180.SH)宣布,由公司自主研发的抗PD-1单抗药物特瑞普利单抗(欧洲商品名:LOQTORZI®)于近日获得欧盟委员会(EC)批准用于治疗两项适应症:
- 特瑞普利单抗联合顺铂和吉西他滨用于复发、不能手术或放疗的,或转移性鼻咽癌(NPC)成人患者的一线治疗;
- 特瑞普利单抗联合顺铂和紫杉醇用于不可切除的晚期/复发或转移性食管鳞癌(ESCC)成人患者的一线治疗。
2024年7月,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)发布积极审评意见,建议批准特瑞普利单抗用于以上两项适应症。此次获批适用于欧盟全部27个成员国以及冰岛、挪威和列支敦士登,使得特瑞普利单抗成为欧洲首个且唯一用于NPC治疗的药物,也是欧洲唯一用于不限PD-L1表达的晚期或转移性ESCC一线免疫治疗药物。
本次EC对于NPC和ESCC适应症的批准分别基于JUPITER-02(一项随机、双盲、安慰剂对照、国际多中心Ⅲ期临床研究,NCT03581786)和JUPITER-06(一项随机、双盲、安慰剂对照、多中心的Ⅲ期研究,NCT03829969)的研究结果。
其中,JUPITER-02是鼻咽癌免疫治疗领域首个国际多中心、样本量最大的双盲、随机对照Ⅲ期临床研究,也是全球首个鼻咽癌一线免疫联合化疗对比单纯化疗将总生存期(OS)预设有统计学检验(一类错误控制)并确证具有生存获益的Ⅲ期临床研究。其研究结果曾以口头报告形式亮相2021年美国临床肿瘤学会(ASCO)年会全体大会(#LBA2),随后荣登《自然-医学》(Nature Medicine,影响因子:58.7)杂志封面,并获得《美国医学会杂志》(Journal of the American Medical Association,JAMA,影响因子:63.1)全文发表。研究结果显示,与单纯化疗相比,特瑞普利单抗联合化疗使患者的疾病进展风险降低48%,死亡风险降低37%。特瑞普利单抗联合化疗组的中位无进展生存期(PFS)对比单纯化疗延长了13.2个月,从8.2个月提升到21.4个月。此外,接受该联合疗法治疗的患者可获得更高的客观缓解率(ORR),更长的持续缓解时间(DoR)和更高的疾病控制率(DCR),且未发现新的安全性信号。长期生存随访数据在2024年ASCO年会展示,特瑞普利单抗治疗组5年生存率达到52.0%。
基于该项研究,特瑞普利单抗分别于2021年和2023年获得国家药品监督管理局(NMPA)和美国食品药品监督管理局(FDA)批准用于晚期鼻咽癌的治疗,是全球首个获批鼻咽癌治疗的免疫检查点抑制剂(ICI)药物,也是美国首个且唯一用于鼻咽癌治疗的药物。此外,特瑞普利单抗用于治疗NPC相关适应症的上市申请正在同步接受英国药品和保健品管理局(MHRA)、澳大利亚药品管理局(TGA)、新加坡卫生科学局(HSA)以及中国香港卫生署药物办公室(DO)等国家和地区监管机构的审评。
JUPITER-06是一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究(NCT03829969),旨在评估与安慰剂联合化疗相比,特瑞普利单抗联合紫杉醇/顺铂(TP)用于晚期ESCC一线治疗的疗效及安全性。该研究结果首次在欧洲肿瘤内科学会年会(ESMO 2021)上以口头汇报形式报告,随后在国际顶尖肿瘤学杂志《Cancer Cell》(影响因子:48.8)和《临床肿瘤学杂志》(Journal of Clinical Oncology,影响因子:42.1)发表。研究结果显示,特瑞普利单抗联合化疗可使晚期或转移性ESCC患者获得更优的PFS和OS,其中中位OS延长6个月,达到17个月,并显著降低患者的疾病进展或死亡风险达42%,显著改善生存获益,且无论PD-L1表达如何均可获益。
基于该项研究,2022年5月,特瑞普利单抗用于治疗ESCC的新适应症上市申请在中国获批。目前,特瑞普利单抗用于一线治疗ESCC的上市申请正在接受MHRA的审评。
JUPITER-02、JUPITER-06主要研究者、中山大学肿瘤防治中心徐瑞华教授表示:"鼻咽癌和食管癌都具有亚洲区域高发的特点,欧美国家在此类瘤种领域的创新疗法开发方面较为缓慢。JUPITER-02和JUPITER-06研究的出色的研究成果证明了在鼻咽癌和食管癌领域,中国学者的诊疗能力和临床科研水平已经位列全球领先,期待这项‘中国方案'能够切实改变国际上罹患这两类瘤种且缺乏有效治疗手段的患者境遇,为他们带来更好的生存希望!"
君实生物总经理兼首席执行官邹建军博士表示:"‘立足中国,布局全球'是君实生物创立之初即确立的战略发展目标,此次特瑞普利单抗获得EC批准,意味着继中国、美国之后,我们全球商业化布局的脚步正式迈向欧洲,也标志着我们在创新药的研发和生产质量再次获得国际权威监管机构的认可。未来,我们将继续携手合作伙伴,全力推动特瑞普利单抗在欧洲地区的商业化落地,为更多海外患者提供来自中国的高质量创新药物
|
1. 本材料旨在传递前沿信息,无意向您做任何产品的推广,不作为临床用药指导。 |
|
2. 若您想了解具体疾病诊疗信息,请遵从医疗卫生专业人士的意见与指导。 |